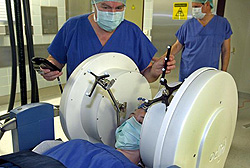
Klinische Prüfung von Medizinprodukten angleichen
Die Bundesregierung will die Sicherheit der Patienten bei der Anwendung von Medizinprodukten wie beispielsweise Kathetern oder Herzschrittmachern verbessern. Die bisher unterschiedlichen Voraussetzungen für klinische Prüfungen von Arzneimitteln und Medizinprodukten sollen angeglichen und die Zuständigkeiten im Bundesinstitut für Arzneimittel und Medizinprodukte zentralisiert werden. Der Gesundheitsausschuss befasst sich am Montag, dem 11. Mai 2009, in einer öffentlichen Anhörung mit dem Thema und wird dazu 24 Verbände und drei Einzelsachverständige befragen.
Laut Gesetzentwurf (
16/12258) soll die Genehmigung durch eine
Bundesoberbehörde sowie eine zustimmende Bewertung der
Ethik-Kommission der Bundesregierung Voraussetzung für eine
klinische Prüfung sein. Bei Meinungsverschiedenheiten
über die Einstufung und Klassifizierung von Medizinprodukten
soll künftig das Bundesinstitut statt der
Länderbehörden abschließend entscheiden.
28 Anmerkungen des Bundesrats
Der Bundesrat hat in seiner Stellungnahme ( 16/12676) 28 Anmerkungen zu dem Gesetzentwurf gemacht. In ihrer Gegenäußerung dazu hat sich die Regierung weitgehend zustimmend zu Änderungsvorschlägen der Länderkammer geäußert.
Zeit: Montag, 11. Mai 2009, 13.00 bis 15.00
Uhr
Ort: Berlin, Reichtstagsgebäude, Saal 3
S 001 (SPD-Fraktionssaal)
Interessierte Besucher, die an den Anhörungen als
Zuhörer teilnehmen möchten, können sich beim
Sekretariat des Ausschusses (Telefon: 030/227-32407, Fax:
030/227-36724, E-Mail:
gesundheitsausschuss@bundestag.de) unter
Nennung des Geburtsdatums und der Personalausweis- oder
Reisepassnummer anmelden.
Bild- und Tonberichterstatter werden gebeten, sich beim
Pressereferat (Telefon: 030/227-32929 oder 32924)
anzumelden.